微小残留病灶检测(MRD)
什么是MRD
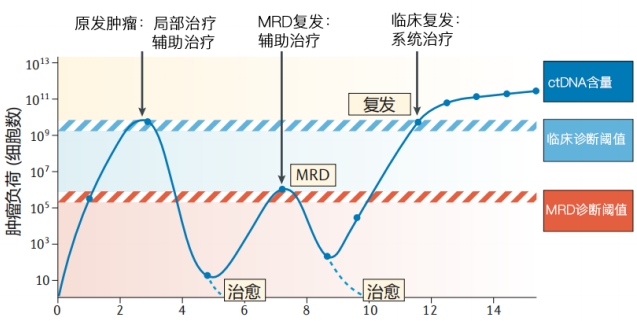
癌症MRD(Minimal Residual Disease),微小残留病灶, 是指在癌症治疗期间或之后,尚未治愈或复发,体内仍残留少量癌 细胞。这些残留的癌细胞无法通过PET或CT扫描等成像技术检测到 ,而且患者通常没有明显的临床症状,因此导致贻误治疗时机。
临床应用
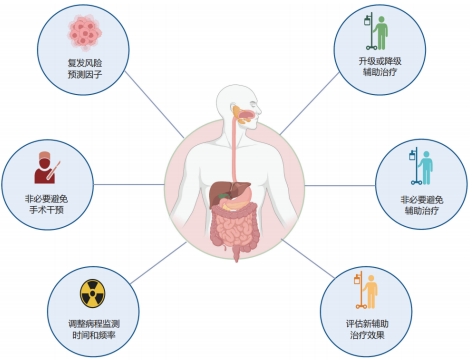
对实体肿瘤患者而言,MRD检测可以帮助临床指导 预后分层、早期干预、辅助治疗、疗效监测和复发监测。
实体瘤MRD如何检测?ctDNA是有效的标志物
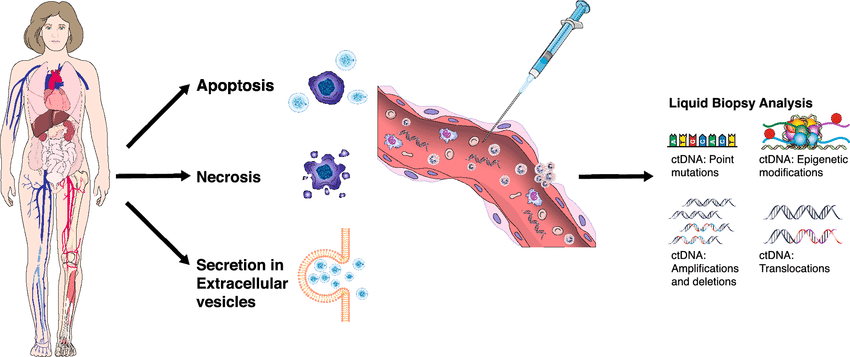
ctDNA即循环肿瘤DNA(circulating tumor DNA),主要由死亡的肿瘤细胞释放或肿瘤细胞分泌,在血液中半衰期约为数小时。ctDNA 携带了丰富的肿瘤DNA变异信息,其变异情况与肿瘤组织的基因变异情况具有高度一致性,因此,ctDNA的检测是识别MRD的最主要的方法, 用作治疗后是否存在残留病灶的实时指标。
指南共识认可
- ● 《2022年中国肺癌高峰论坛专家共识》
- ● 《结直肠癌分子检测高通量测序专家共识》
- ● 《ctDNA高通量测序临床实践专家共识(2022版)》
- ● 《基于靶标指导乳腺癌精准治疗标志物临床专家共识(2022版)》
- ● 《肺癌分子(微小)残留病灶(MRD)的检测和临床应用共识》
ctDNA检测难点
含量低
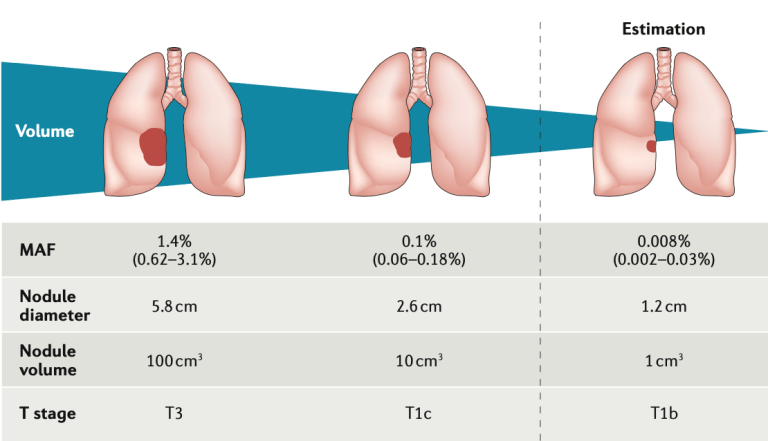
ctDNA含量与肿瘤负荷正相关,肿瘤越大血浆中ctDNA含量越高。因此在肿瘤复发早期,肿瘤细胞量比较少,血浆中的ctDNA含量极低,可达万分位乃至十万分位水平。因此需要检测方法具备检测十万分位含量ctDNA的能力,同时对方法的准确性要求极高,错误率要低于十万分位。
解决方案
- 1、采用超高测序深度,增加检测灵敏度;
- 2、检测多个位点,增加ctDNA检出的几率;
- 3、采用高效的纠错技术,增加检测的准确性
假阳性
克隆性造血(clonal hematopoiesis,CH)突变是造血干细胞携带的突变。其含量与ctDNA相当甚至高于ctDNA含量。因此使用ctDNA进行MRD检测时,CH突变与真实的肿瘤来源体细胞突变无法被区分,导致结果的假阳性。因此需要去除CH突变的干扰。
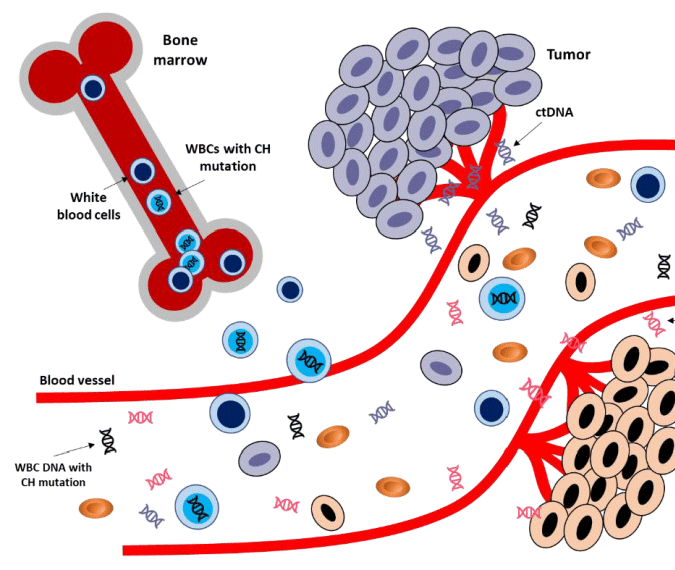
- 1、对肿瘤组织DNA与正常组织DNA进行平行测序,鉴定出真实的体细胞变异,用于MRD检测。
MRD-ctDNA检测技术路线
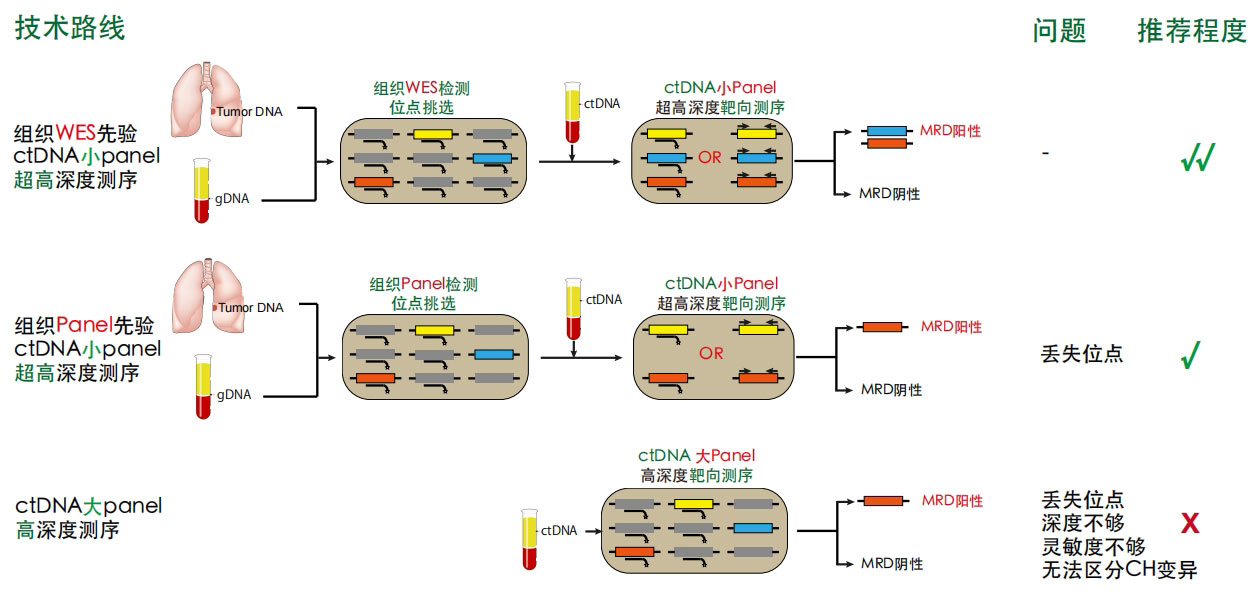
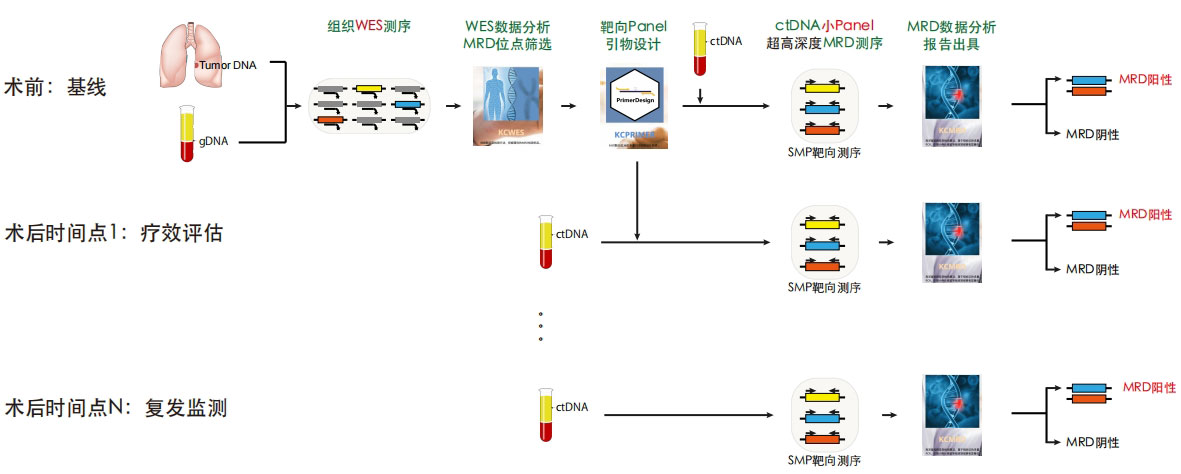
康测科技MRD检测技术路线
康测科技MRD检测,采用组织先验的方式,提供可靠的MRD位点来源信息,同时有效过滤克隆性造血引入的假阳性;组织先验采取WES检测,覆盖所有19000多个编码基因,不遗漏任何有价值的位点;配合高性能KCPrimer引物设计平台,快速合成任意位点的MRD检测用panel;MRD检测采用先进的SMP靶向建库技术,LoD可达0.005%(十万分之五),灵敏度、特异性均为 100%。
样品采集方案

检测流程
检测周期:
首次检测:组织WES报告 + 定制化成功通知 15个自然日
持续监测:ctDNA检测 10个自然日
康测科技MRD检测产品优势
- • 组织先验:提供可靠的MRD位点,彻底去除克隆性造血引入的假阳性
- • WES先验:覆盖19000+编码基因,不错过任何有价值的位点
- • 基于mPCR技术平台:经济、快速、灵活、稳定
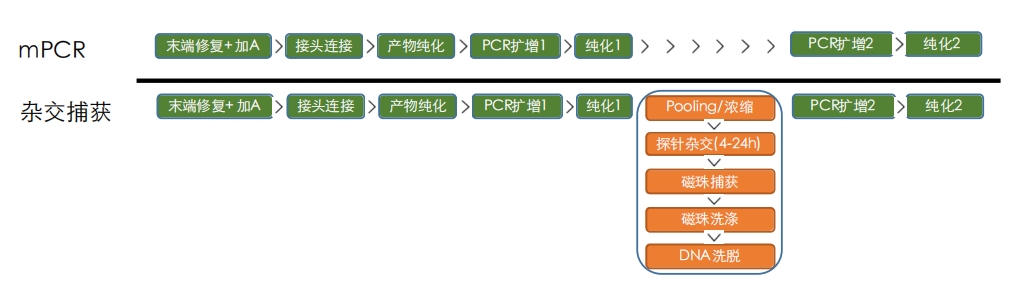
- • 超高深度测序:100000x 以上测序深度,稳定检出十万分之三的突变
- • 基于SMP纠错技术:LoD ≥ 0.005%(十万分之五),Sensitivity&Specificity = 100%
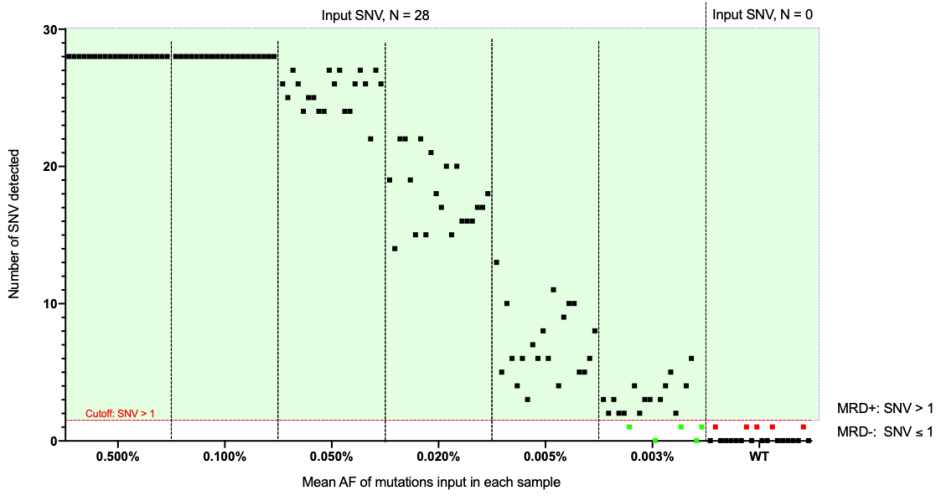
康测MRD建库试剂盒,使用三个商业化标准品(菁良基因GW-OCTM800、LDT Bioscience LDT-999和科佰生物CBP940)进行了300次性能验证,在使用SNV Cutoff > 1的条件下,实现了 100%的特异性。
对十万分之五含量的ctDNA检测结果,每个样本平均检出7.1个变异(最少4个),远高于1。在对十万分之三含量的ctDNA检测中,20个阳性样本中有15个检测到≥2个变异,为MRD阳性。
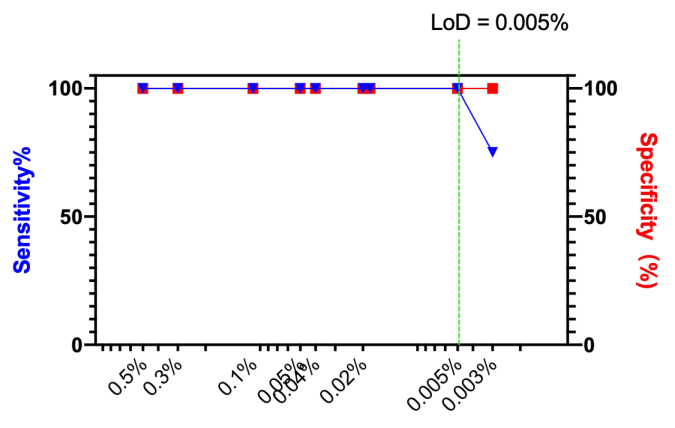
综合所有测试结果,我们发现使用cutoff > 1的阈值,所有检测的Specificity均可达到100%。在十万分之五的 ctDNA含量下,Sensitivity也稳定在100%,十万分之三含量Sensitivity为75%(未达95%)。因此我们将该试剂盒的报告阈值定义为SNV > 1, LoD计算为十万分之五。
康测MRD检测核心技术:SMP靶向测序技术
Stranded Multiplex PCR
| 工作流程 | 错误来源 | 错误率 |
|---|---|---|
| 样本处理 | DNA损伤,如8-oxoG | |
| 文库PCR扩增 | 早期掺入错误和聚合酶偏好性 | 0.6‰[1] |
| 测序 | 测序错误 | 1‰ |
二代测序技术(NGS)在样本处理、文库制备和测序过程中均会产生不同几率的错误,累积背景错误率在1‰左右。在检测含量在1‰及以下的突变中,真实突变水平接近甚至低于背景错误,无法被有效区分,因此无法直接应用。如肿瘤患者血液中ctDNA的突变,含量在1‰以下,通常在1‰~0.1‰的水平。因此需要高效的纠错技术去除背景错误,以鉴定真实变异。
SMP靶向测序技术
为此,我们开发了SMP(链特异性多重PCR)靶向测序技术。SMP是一种基于不对称多重PCR平台、同时又拥有双链纠错能力的靶向测序技术。其核心在于创新性的引入了3标签体系。
该技术在每一个DNA双链分子的一端同时添加两种标记:一个UMI标记用于区分不同DNA,两个链分子标签(strand identifiers, SID)用于区分同一DNA的正链和负链。在单侧多重引物扩增之后,同一DNA的正链和负链带有相同的UMI标记,和不同的SID标记。分析时,通过UMI确定同一来源的DNA分子,再通过SID确定其链的来源,即可区分同一DNA分子的正链序列负链序列。通过还原正负链即可过滤掉所有的假阳性变异和检测错误。

SMP纠错性能
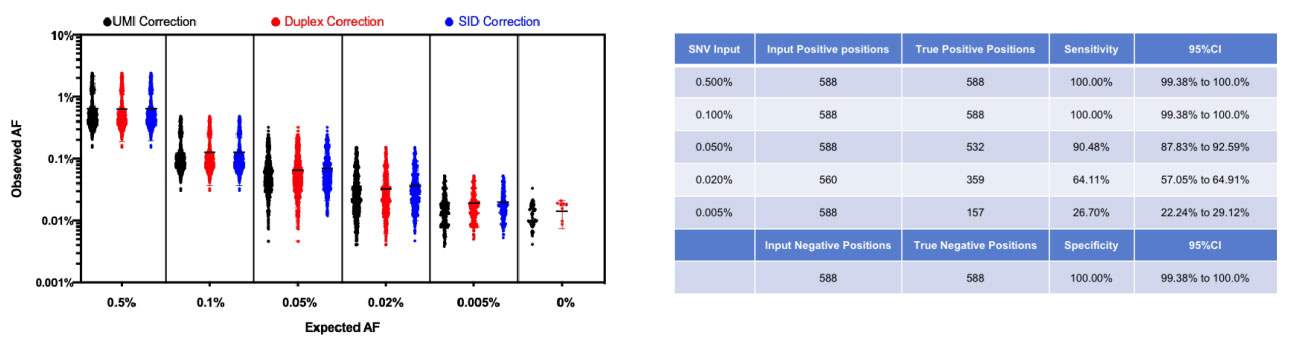
我们使用菁良科技的质控品GW-OCTM800对技术性能进行了验证,该质控品含有37个热点突变,突变频率为0%、0.005%、0.05%和0.5%。我们使用该质控品,进一步稀释,形成突变频率为0%、0.005%、0.02%、0.05%、0.1%和0.5%的6个梯度,选择了28个位点,使用SMP技术进行了21次的重复检测。结果如上图左所示:普通UMI纠错无法过滤掉所有错误,UMI纠错后0%样品(无突变)存在大量的假阳性变异(34个);SMP技术的SID分子内双链纠错,则可以完全去除0%样品中的假阳性,且对阳性样本的灵敏度影响不大。
使用SID纠错,对数据进行进一步分析,发现SMP技术的检测限低于十万分之五:在特异性100%的条件下,对1‰及以上含量的突变灵敏度达到100%,万分之二的灵敏度高达64%,对十万分之五含量的突变,灵敏度仍高达26.7%(上图右)。
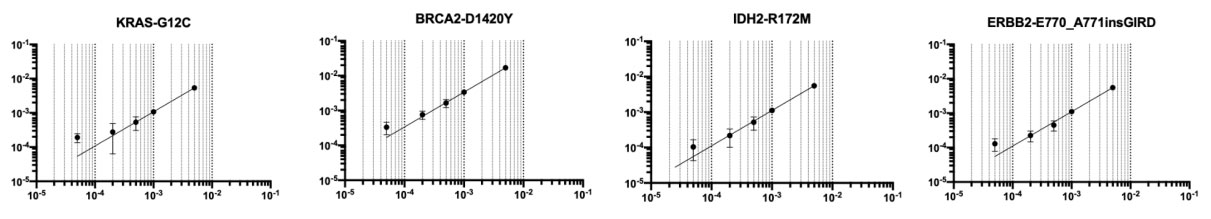
SMP定量准确性
我们选取了部分位点进行展示,可见SMP定量非常准确,从十万分位到百分位,表现出良好的线性关系。
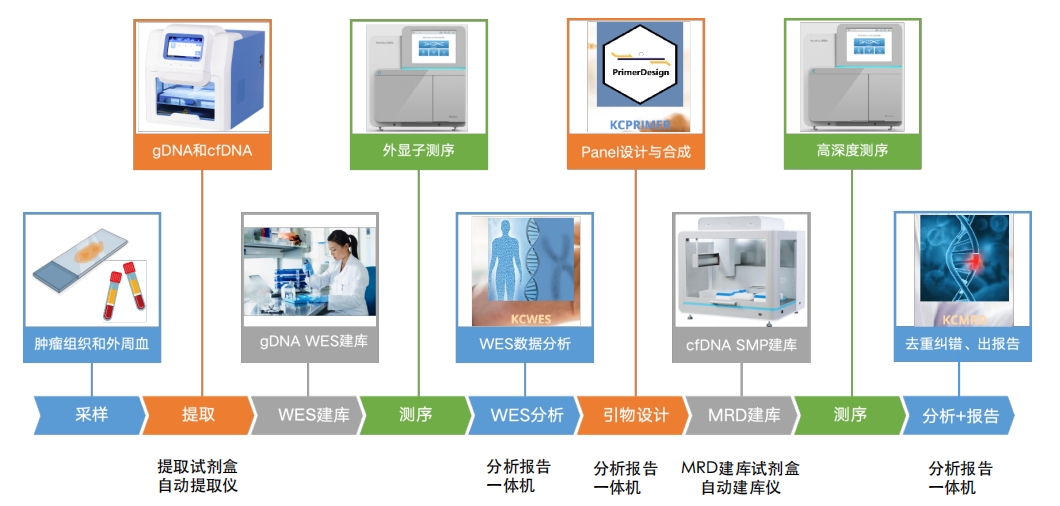
MRD一站式自动化解决方案
自建MRD检测平台的SMP靶向技术

康测MRD一站式解决方案
灵敏准确、自主无忧、省心高效

• 定制自动核酸提取仪 + 自研试剂盒

- 适用范围广:兼容200 μL ~ 10 mL
- 提取速度快:50 min内完成1 ~ 24个血浆样品提取
- 核酸得率高:在竞品中名列前茅
- 操作简单:预分装试剂、预设程序,一键启动,无人值守
• 分析报告一体机
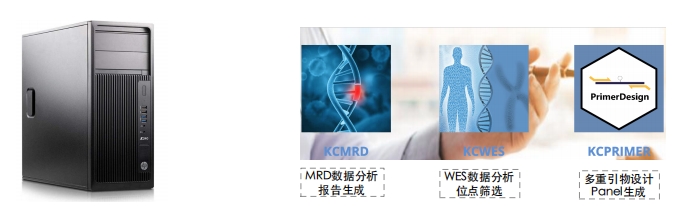
- 全流程:内置KCWES、KCPrimer和KCMRD模块,满足从 WES分析、位点筛选、panel设计、MRD数据分析到报告生成的全流程
- 高效:2h完成WES分析和位点筛选、5min完成Panel设计,2h出具MRD报告
- 易用:流程间无缝衔接,全图形界面,设置简单易上手,无需编程
- 安全:本地运行、数据本地储存,保证隐私和数据安全
- 可定制:报告可自主定义企业信息,定制专属检测报告模板
分析报告一体机使用流程
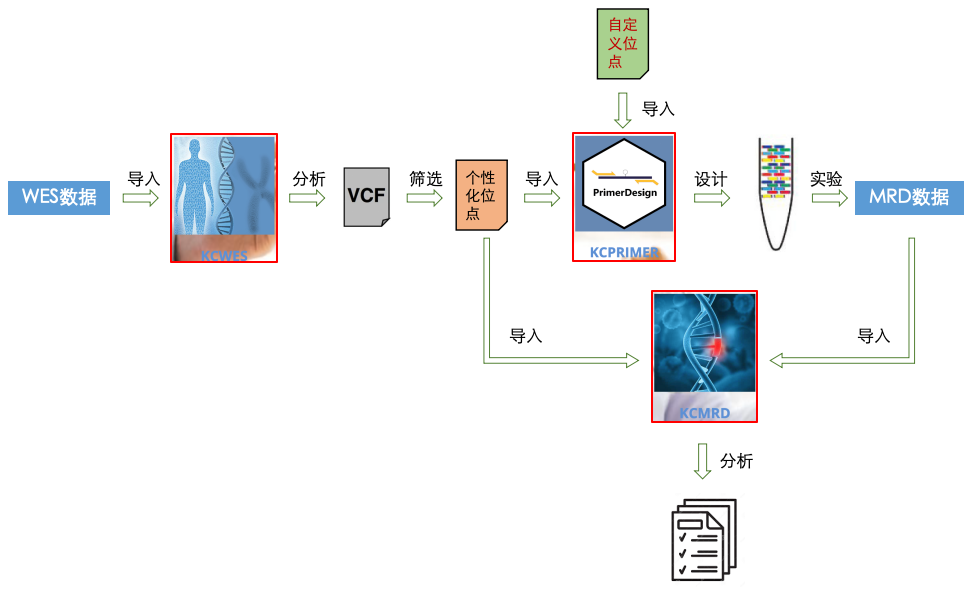
• 分析报告一体机之mPCR靶向Panel定制系统

本系统为“分析报告一体机”的核心功能之一。其主要功能为根据提供的待检测位点列表,设计用于不对称多重PCR的Tag引物池。该引物池合成后,和内参引物一起,对添加了SMP接头的DNA进行多重PCR靶向扩增,最终形成SMP测序文库。本系统对每一个待检测位点同时设计F和R两条引物, 均带有illumina的P7 tag,F和R组合不 扩增,仅分别和SMP接头上的P5 Tag 扩增。
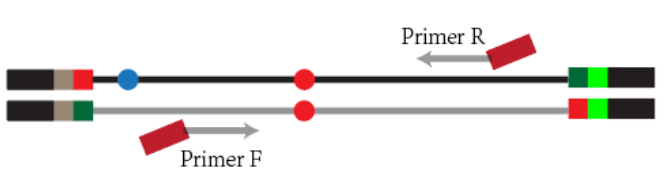

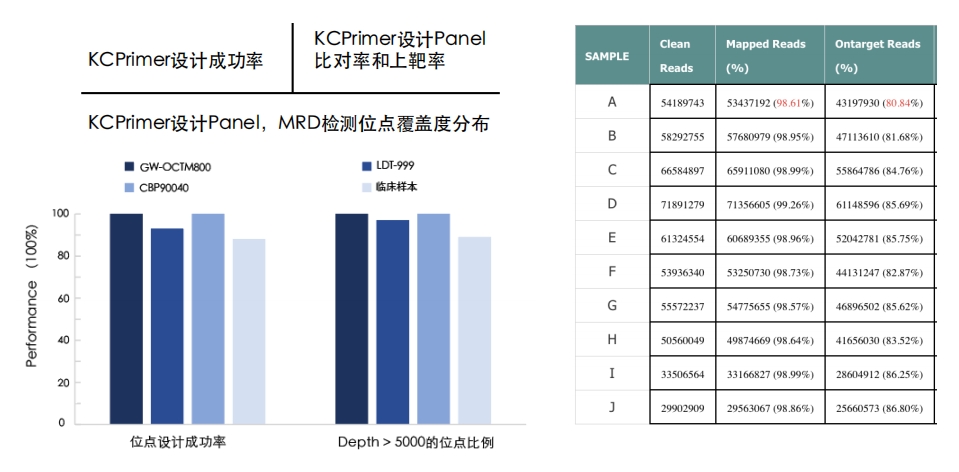
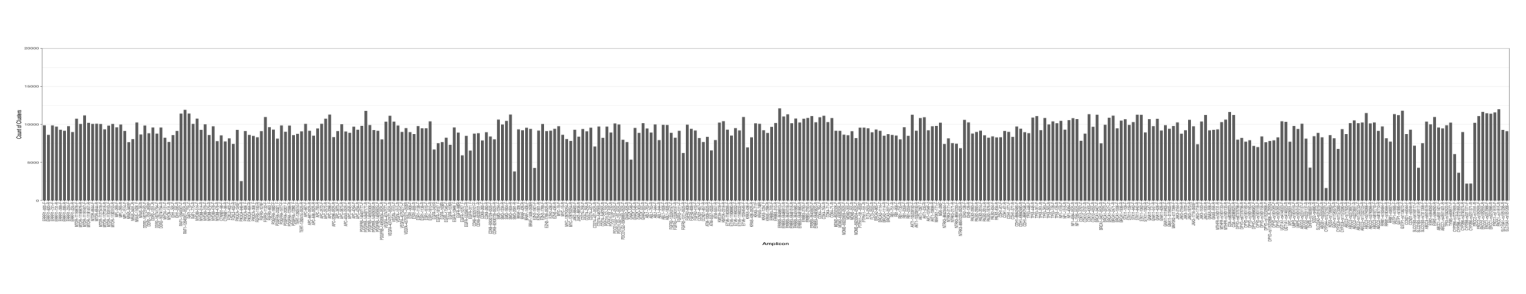
KCPrimer靶向Panel定制系统性能

了解更多

武汉康测医学检验有限公司
Wuhan Kangce Medical Inspection Co., Ltd
地址:武汉市江夏区东湖新技术开发区高新六路99号南山·光谷自贸港D2栋
电话:027-65563640 邮箱:medical@seqmed.cn 网址:www.seqmed.cn

